グループ担当教員: 林 泰弘 特任助教
グループ担当教員: 林 泰弘 特任助教
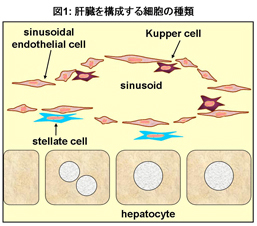
肝臓は、胆汁の産生、炭水化物、脂質、たんぱく質の代謝、解毒作用、アルブミンの合成、血糖値の合成など全身の代謝の恒常性の中心を担うとても重要な臓器です。これらの機能は主に肝臓の実質細胞(hepatocyte)で行われており、肝臓の細胞の約80%を占めています。そして残りの20%は非実質細胞(non-parenchymal cells)で構成されており、血管内皮細胞(endothelial cells)、クッパー細胞(kupper cells)、そして星細胞(stellate cells)などに分けられます(図1)。
肝臓の機能異常は、脂肪肝、肝硬変、肝炎、糖尿病などといった重篤な病気の引き金となります。これらの病気の多くは肝臓が炎症状態になっており、様々な細胞からサイトカイン類が分泌されています(Table1; Ramadori G et al. J Physiol Pharmacol. 2008より抜粋)。サイトカイン類の異常分泌と病気の発症との関連性についてはまだ不明な点も多いですが、肝炎、肝硬変の成立には血管内皮細胞の異常が関与していることが明らかになっております。

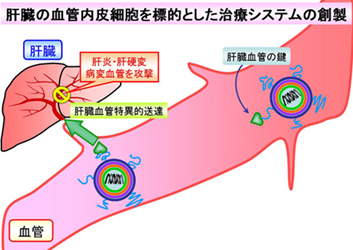
薬剤分子設計学研究室では、独自の人工遺伝子ベクターである多機能性エンベロープ型ナノ構造体(MEND)を用いた、肝機能疾患治療用の静脈内投与型デリバリーシステムの構築に向けた研究を行っています(薬剤分子設計学研究室テーマ:肝機能疾患治療用静脈内投与型デリバリーシステムの構築参照)。そこで未来創剤学研究室の肝臓グループでは、肝臓の血管内皮へ薬物や治療用核酸を効率的に送達可能なDDS(drug delivery system)の開発を行います。肝臓血管内皮に選択的なリガンドをMENDに修飾することで各細胞に効率的に送達可能なシステムの構築を目指します。最終的には肝炎、肝硬変といった肝臓の疾患を治療可能なシステムの構築を行い、次世代型の治療薬の創製を目指します。