アジュバント搭載ナノDDSの開発
Programmed cell death 1(PD-1)抗体に代表される免疫チェックポイント阻害剤は、がん治療に革命をもたらしました。しかしながら、その効果は一部の患者に限られており、全ての患者に効果があるわけではありません。免疫チェックポイント阻害剤が無効な患者の多くはがんに対する免疫応答が活性化していない場合が多いため、がんに対する免疫応答を活性化させる薬剤との併用が有用であると考えられています。免疫を活性化させる物質はアジュバント(免疫賦活化剤)と呼ばれ、がんや感染症に対する免疫応答を活性化する目的で研究開発が進められています。しかしながら、アジュバントの多くは分解性や難溶性の観点から、単体では十分に機能を発揮することができません。そこで、我々はナノサイズのキャリア型drug delivery system(ナノDDS)にアジュバントを搭載することで、がんに対する免疫応答を効率的に活性化させる研究を行っています。アジュバントを独自のナノDDSに搭載することで、がん免疫応答応答の増強、アジュバントの毒性軽減、免疫チェックポイント阻害剤との相乗効果の誘導などに成功しています。
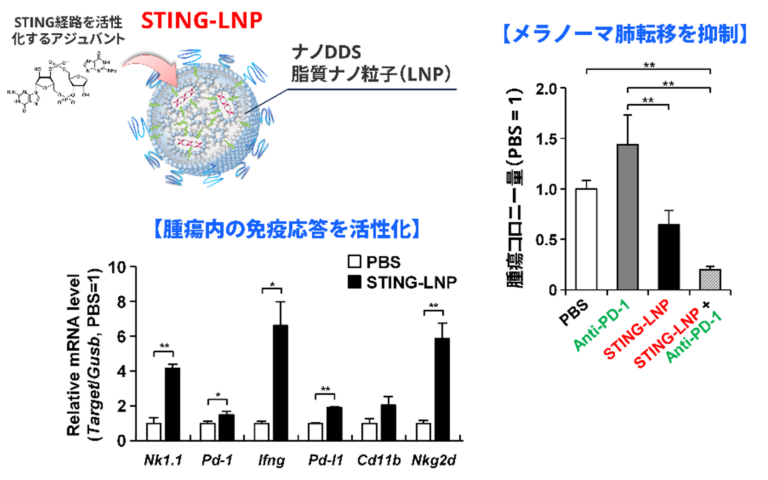
NK細胞の機能制御に基づいたナノがん免疫療法の開発
現在のがん免疫療法の主役は、がん細胞を特異的に認識して傷害するT細胞です。この特異的なT細胞は、がん抗原を取り込んだ樹状細胞からの抗原提示を受けて活性化し、がん細胞上に提示されるがん抗原を認識することで特異的に傷害します。一方で、がん細胞は変異を繰り返すことで、がん抗原の消失、抗原提示の阻害など巧みなメカニズムを獲得することでT細胞からの攻撃を回避し、がん免疫療法に対する耐性を生み出します。このようなT細胞に耐性を持ったがんに対して、有効だと期待されているのがnatural killer(NK)細胞です。T細胞とは異なり、NK細胞はがん抗原に依存せずに異常な細胞を傷害することが可能です。我々は、ナノDDS技術を用いてNK細胞の機能を改変するための核酸(siRNAやmRNA)をNK細胞へと送達し、機能を改変することでNK細胞を強化する研究を進めています。NK細胞への核酸送達は非常に難易度が高いのですが、従来技術を遥かに凌駕する効率でsiRNAやmRNAを送達することに成功し、がんに対するNK細胞療法の効果を増強できることを明らかにしています。
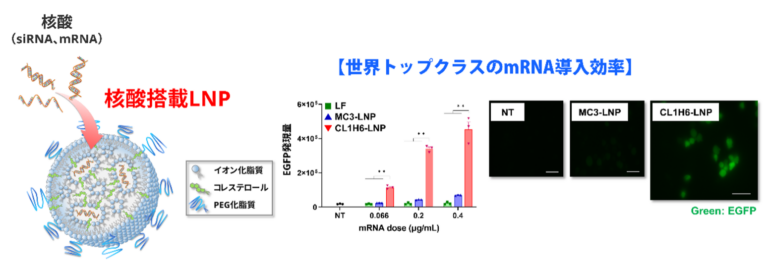
サブセットレベルで細胞を識別する標的化技術の開発
近年のシングルオミクス解析技術の発展により得られた詳細な細胞の多様性は、様々な疾患の詳細なメカニズムを明らかにし、様々な細胞サブセットが関与していることが示されています。それ故、細胞サブセットが医薬品の標的として重要になることが予想されます。しかしながら、細胞をサブセットレベルで識別し、選択的に薬物を送達可能なactive targeting技術の報告はありませんでした。我々は独自のactive targeting技術を発明し、サブセットレベルで細胞を判別可能なナノDDSシステムの開発に関する研究を進めています。この技術の開発は、今後の医薬品開発を大きく加速することに繋がります。
腫瘍血管破壊に基づいた新規がん治療法の開発
最近、我々はsiRNAを腫瘍血管内皮細胞(tumor endothelial cell: TEC)へと送達することで機能制御可能なナノDDSとアジュバント搭載ナノDDSの2つを組み合わせることで、急速な腫瘍血管の破壊を誘導し、強力ながん治療効果を示すことを発見しました。本併用療法は、免疫チェックポイント阻害剤に耐性を示すマウス腫瘍に対しても有効であり、実用化されている血管新生阻害剤よりも強力な治療効果を示します。さらに、ヒト膵臓がんモデルなど複数のヒト腫瘍に対しても治療効果を示したことから、高いポテンシャルを用いたがん治療法であると期待できます。現在は、薬効メカニズムの解明や処方の最適化を進め、新しい機序の創薬シーズとしての確立を目指しています。
