Research
研究内容
1. スフィンゴ脂質関連遺伝子の同定
脂質の生合成・代謝に関わらず,生体内の殆ど全ての化学反応は酵素により触媒されている。 各反応を触媒する酵素の遺伝子を同定することはその後の生化学,分子生物学,遺伝学,生理学,病態解析に極めて重要である。 例えば,遺伝子欠損体の作成はその遺伝子(あるいは遺伝子産物であるタンパク質)とそのタンパク質生成物(生化学研究室の場合は脂質分子)の生理機能,病態における役割の解明に役立つ。 リコンビナントの作成は,酵素の大量発現・精製とin vitro における解析,抗体の作成などに有用である。
生化学研究室(旧生体機能化学研究室を含む)ではこれまでに数多くのスフィンゴ脂質関連遺伝子を同定してきた。 これらには,長鎖塩基/セラミド合成,長鎖塩基/長鎖塩基1-リン酸分解経路(詳細は「2. 長鎖塩基の代謝経路と脂肪酸 α 酸化経路の解明」を参照),極長鎖脂肪酸伸長経路(詳細は「3. 極長鎖脂肪酸の産生,生理機能,病態」を参照),アシルセラミド合成経路(詳細は「4. セラミドによる皮膚バリア形成」を参照),その他に分けられる。 図4にセラミド代謝経路と生化学研究室で同定した遺伝子群(赤,哺乳類遺伝子;青,酵母遺伝子)を示す。
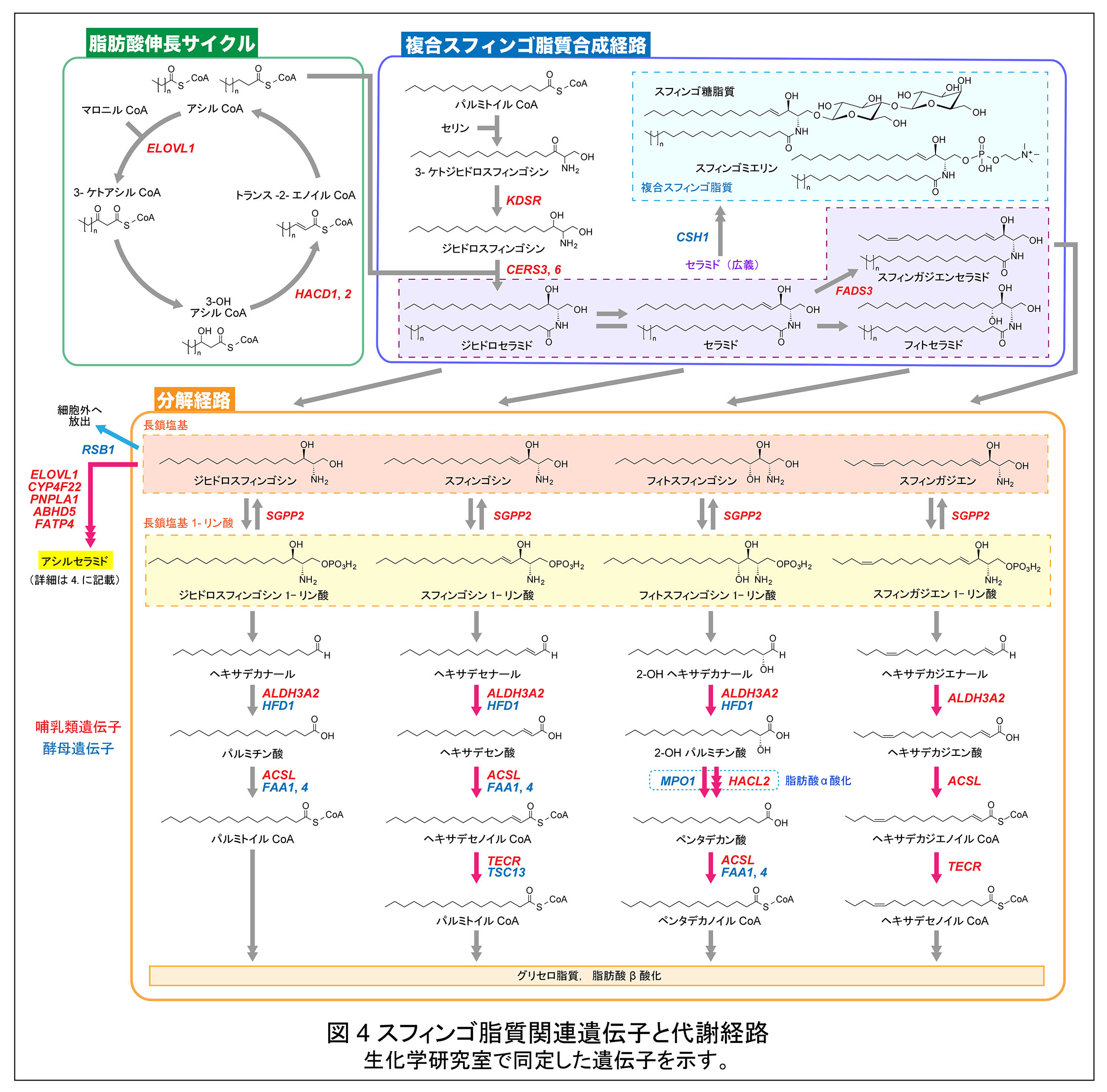
生化学研究室で同定・機能解明した遺伝子
長鎖塩基/セラミド合成関連
- 3-ケトジヒドロスフィンゴシン還元酵素 KDSR (哺乳類): KDSR (別名 FVT-1)がスフィンゴ脂質合成の第二段階である 3-ケトジヒドロスフィンゴシンからジヒドロスフィンゴシンへの変換を担う酵素であることを解明した1)。KDSR 遺伝子変異が道化師様魚鱗癬を引き起こすことを見出した2) 。
- セラミド不飽和化酵素 FADS3 (哺乳類): スフィンガジエン(4,14-スフィンガジエン)に特徴的な 14 位シス二重結合を導入する酵素遺伝子としてFADS3 を同定した3) 。FADS3 の基質が長鎖塩基ではなくセラミドであることを含む,酵素学的性質および代謝経路の詳細を解明した31) 。
- セラミド合成酵素 CERS3 (哺乳類): CERS3 (別名 LASS3)がセラミド合成酵素であることを初めて報告するとともに4) ,ケラチノサイトの分化依存的に発現が上昇することを見出して皮膚におけるセラミド産生に重要なことを示唆した30) 。CERS3 変異をもつ魚鱗癬患者の解析から,アシルセラミド低下が魚鱗癬発症に直接関与することを明らかにした31) 。
- セラミド合成酵素 CERS6 (哺乳類): CERS6(別名 LASS6)がC16:0 アシル CoA に高い基質特異性を示すセラミド合成活性を示すことを初めて報告した5) 。
長鎖塩基/長鎖塩基1-リン酸分解経路関連
- アルデヒドデヒドロゲナーゼ ALDH3A2, ALDH3B2(哺乳類)/HFD1(酵母):長鎖塩基 1-リン酸の S1P リアーゼによる分解産物である長鎖アルデヒドを長鎖脂肪酸へ変換することを解明した 6)。その実験的根拠として,酵母の各アルデヒドデヒドロゲナーゼ遺伝子欠損株の解析から HFD1 の欠損株でのみ長鎖塩基分解経路が停止すること,さらにその哺乳類ホモログである ALDH3A2 の哺乳類培養 KO 細胞中でも同様に長鎖塩基分解が停止することを明らかにした。ALDH3A2 と同じ ALDH3 ファミリーに属する ALDH3B2 はヒトでは偽遺伝子だが,マウスでは ALDH3A2 とともに長鎖塩基分解経路において働くことを,Aldh3a2 KO マウスや Aldh3a2 Aldh3b2 二重 KO マウスの解析から明らかにした32, 33) 。ALDH3A2 は神経皮膚疾患であるシェーグレン・ラルソン症候群(SLS)の原因遺伝子である。SLS 患者角質層のセラミドプロファイリングを行い,アシルセラミド量の低下が皮膚病態を引き起こすことを解明した34) 。
- アシル CoA 合成酵素 ACSL1,3,4,5,6(哺乳類)/FAA1, FAA4(酵母):ALDH3A2/Hfd1 によって産生された長鎖脂肪酸をアシル CoA へ変換することを解明した6, 7) 。酵母の各アシル CoA 合成酵素遺伝子の単独あるいは二重欠損株を用いた解析から faa1Δ faa4Δ 株中で長鎖塩基の分解経路が遮断されること,および哺乳類培養細胞においても ACSL 阻害剤処理により同様の結果が得られることを明らかにした。
- トランス-2-エノイル CoA 還元酵素 TECR(哺乳類)/TSC13(酵母):スフィンゴシン/スフィンゴシン1-リン酸の分解経路で生じたヘキサデセノイル CoA (トランス-2-ヘキサデセノイル CoA )を飽和化し,パルミトイル CoA を産生することを解明8)。TECR は非症候性精神遅滞の原因遺伝子。別名 TER。
- 2-ヒドロキシ脂肪酸ジオキシゲナーゼ MPO1(酵母):フィトスフィンゴシンの代謝過程において生じた 2-ヒドロキシ脂肪酸を1炭素短い脂肪酸へ変換(α 酸化)する遺伝子としてリバースジェネティクスにより同定9)。Metabolism of Phytosphingosine to Odd-numbered fatty acids から命名。その後の解析から,鉄イオンを捕因子とするジオキシゲナーゼであることを解明10)。IUPAC に EC 1.14.18.12 として登録。
- 2-ヒドロキシアシル CoAリアーゼ HACL2(哺乳類):フィトスフィンゴシンの代謝過程において生じた 2-ヒドロキシアシル CoA を1炭素短い長鎖アルデヒドへ変換(α 酸化)することを 2-ヒドロキシ分岐鎖アシル CoA に活性を示す HACL1 との相同性から同定11)。
脂肪酸伸長サイクル関連
- 脂肪酸伸長酵素(エロンガーゼ)ELOVL1(哺乳類):脂肪酸伸長サイクル1段回目のアシル CoA とマロニル CoA の縮合反応を担う。C20-C22 アシル CoA を C24-C26 アシル CoA へ伸長させる活性をもつことを解明12)。皮膚では超長鎖セラミドやアシルセラミド産生に重要であり,皮膚バリア形成に関与13)。眼においては極長鎖マイバム脂質の産生に関与し,ドライアイを防止14) (プレスリリース原稿)。神経系では極長鎖スフィンゴ脂質(特にガラクトシルセラミドやスルファチド)の産生を通じてミエリン機能に関与15)。神経皮膚疾患である IKSHD 症候群の原因遺伝子16)。
- 3-ヒドロキシアシル CoA 脱水酵素 HACD1,HACD2(哺乳類):脂肪酸伸長サイクル3段回目の脱水反応である 3-ヒドロキシアシル CoA からトランス-2-エノイル CoA の産生を担う遺伝子として酵母 PHS1 との相同性から同定17)。3-Hydroxy Acyl-CoA Dehydratase から命名。HACD2 はミオパチーの原因遺伝子18)。
アシルセラミド合成経路関連
- 脂肪酸ω-水酸化酵素 CYF4F22(ヒト)/Cyp4f39(マウス):シトクローム P450 の一種で C30-C36 の鎖長をもつ超長鎖脂肪酸のω末端を水酸化する活性をもち,アシルセラミド(皮膚)(プレスリリース原稿)や OAHFA などのω-水酸化脂質産生(涙液油層)(プレスリリース原稿)に関わる遺伝子として同定19, 20)。常染色体潜性先天性魚鱗癬の原因遺伝子。
- トランスアシラーゼ PNPLA1(哺乳類):アシルセラミド産生経路において,トリグリセリド中のリノール酸をω-水酸化セラミドへ転移する遺伝子として同定21)。IUPAC に EC 2.3.1.296 として登録。常染色体潜性先天性魚鱗癬の原因遺伝子。(プレスリリース原稿)
- PNPLA1 の反応促進因子 ABHD5(哺乳類):PNPLA1 によるトリグリセリド利用を促進させる役割をもつことを解明22)。症候性魚鱗癬であるシャナリン・ドルフマン症候群原因遺伝子。
- アシル CoA 合成酵素 FATP4(哺乳類):アシルセラミド産生経路において,CYP4F22/Cyp4f39 が産生したω-水酸化超長鎖脂肪酸をアシル CoA へ変換する遺伝子として同定23)(プレスリリース原稿)。別名:ACSVL4。症候性魚鱗癬である魚鱗癬未熟児症候群の原因遺伝子。
その他
- 長鎖塩基トランスロカーゼ RSB1(酵母):長鎖塩基を細胞外へ放出するトランスロカーゼ/トランスポーターとして,酵母を用いた遺伝学(培地中に添加した長鎖塩基に対して耐性を示すマルチコピーサプレッサー)によって同定24)。Resistance to Sphingoid Base から命名。その後の解析により,細胞膜の脂質非対称性に変化が生じると RSB1 の発現が誘導され,そのシグナル伝達には Rim101 経路が関与する(Rim21 が脂質非対称センサー)ことを解明25-27)。
- スフィンゴシン1-リン酸ホスファターゼ SGPP2(哺乳類):スフィンゴシン1-リン酸を脱リン酸化し,スフィンゴシンへ変換。同様の活性をもつSGPP1 とのホモロジーから同定28)。別名 SPP2。
- IPC マンノシルトランスフェラーゼ CSH1(酵母):イノシトールホスホリルセラミド(IPC)にマンノースを転移し,マンノースイノシトールホルホリルセラミド(MIPC)を産生。同様の活性をもつ CSG1 との相同性から同定29)。CSG1 Homology から命名。
研究業績
- Kihara A, Igarashi Y (2004) FVT-1 is a mammalian 3-ketodihydrosphingosine reductase with an active site that faces the cytosolic side of the endoplasmic reticulum membrane. J Biol Chem, 279, 49243-49250.
- Takeichi T, Torrelo A, Lee JYW, Ohno Y, Lozano ML, Kihara A, Liu L, Yasuda Y, Ishikawa J, Murase T, Rodrigo AB, Fernandez-Crehuet P, Toi Y, Mellerio J, Rivera J, Vicente V, Kelsell DP, Nishimura Y, Okuno Y, Kojima D, Ogawa Y, Sugiura K, Simpson MA, McLean WHI, Akiyama M, McGrath JA (2017) Biallelic mutations in KDSR disrupt ceramide synthesis and result in a spectrum of keratinization disorders associated with thrombocytopenia. J Invest Dermatol, 137, 2344-2353.
- Jojima K, Edagawa M, Sawai M, Ohno Y, Kihara A (2020) Biosynthesis of the anti-lipid-microdomain sphingoid base 4,14-sphingadiene by the ceramide desaturase FADS3. FASEB J, 34, 3318-3335.
- Mizutani Y, Kihara A, Igarashi Y (2006) LASS3 (longevity assurance homologue 3) is a mainly testis-specific (dihydro)ceramide synthase with relatively broad substrate specificity. Biochem J, 398, 531-538.
- Mizutani Y, Kihara A, Igarashi Y (2005) Mammalian Lass6 and its related family members regulate synthesis of specific ceramides. Biochem J, 390, 263-271.
- Nakahara K, Ohkuni A, Kitamura T, Abe K, Naganuma T, Ohno Y, Zoeller RA, Kihara A (2012) Sjögren-Larsson syndrome gene encodes a hexadecenal dehydrogenase of the sphingosine 1-phosphate degradation pathway. Mol Cell, 46, 461-471.
- Ohkuni A, Ohno Y, Kihara A (2013) Identification of acyl-CoA synthetases involved in the mammalian sphingosine 1-phosphate metabolic pathway. Biochem Biophys Res Commun, 442, 195-201.
- Wakashima T, Abe K, Kihara A (2014) Dual functions of the trans-2-enoyl-CoA reductase TER in the sphingosine 1-phosphate metabolic pathway and in fatty acid elongation. J Biol Chem, 289, 24736-24748.
- Kondo N, Ohno Y, Yamagata M, Obara T, Seki N, Kitamura T, Naganuma T, Kihara A (2014) Identification of the phytosphingosine metabolic pathway leading to odd-numbered fatty acids. Nat Commun, 5, 5338.
- Seki N, Mori K, Kitamura T, Miyamoto M, Kihara A (2019) Yeast Mpo1 is a novel dioxygenase that catalyzes the α-oxidation of a 2-hydroxy fatty acid in an Fe2+-dependent manner. Mol Cell Biol, 39, e00428-00418.
- Kitamura T, Seki N, Kihara A (2017) Phytosphingosine degradation pathway includes fatty acid α-oxidation reactions in the endoplasmic reticulum. Proc Natl Acad Sci USA , 114, E2616-E2623.
- Ohno Y, Suto S, Yamanaka M, Mizutani Y, Mitsutake S, Igarashi Y, Sassa T, Kihara A (2010) ELOVL1 production of C24 acyl-CoAs is linked to C24 sphingolipid synthesis. Proc Natl Acad Sci USA, 107, 18439-18444.
- Sassa T, Ohno Y, Suzuki S, Nomura T, Nishioka C, Kashiwagi T, Hirayama T, Akiyama M, Taguchi R, Shimizu H, Itohara S, Kihara A (2013) Impaired epidermal permeability barrier in mice lacking the Elovl1 gene responsible for very long-chain fatty acid production. Mol Cell Biol, 33, 2787-2796.
- Sassa T, Tadaki M, Kiyonari H, Kihara A (2018) Very long-chain tear film lipids produced by fatty acid elongase ELOVL1 prevent dry eye disease in mice. FASEB J, 32, 2966-2978.(プレスリリース原稿)
- Isokawa M, Sassa T, Hattori S, Miyakawa T, Kihara A (2019) Reduced chain length in myelin sphingolipids and poorer motor coordination in mice deficient in the fatty acid elongase Elovl1. FASEB Bioadv, 1, 747-759.
- Mueller N, Sassa T, Morales-Gonzalez S, Schneider J, Salchow DJ, Seelow D, Knierim E, Stenzel W, Kihara A, Schuelke M (2019) De novo mutation in ELOVL1 causes ichthyosis, acanthosis nigricans, hypomyelination, spastic paraplegia, high frequency deafness and optic atrophy. J Med Genet, 56, 164-175.
- Ikeda M, Kanao Y, Yamanaka M, Sakuraba H, Mizutani Y, Igarashi Y, Kihara A (2008) Characterization of four mammalian 3-hydroxyacyl-CoA dehydratases involved in very long-chain fatty acid synthesis. FEBS Lett, 582, 2435-2440.
- Muhammad E, Reish O, Ohno Y, Scheetz T, Deluca A, Searby C, Regev M, Benyamini L, Fellig Y, Kihara A, Sheffield VC, Parvari R (2013) Congenital myopathy is caused by mutation of HACD1. Hum Mol Genet, 22, 5229-5236.
- Ohno Y, Nakamichi S, Ohkuni A, Kamiyama N, Naoe A, Tsujimura H, Yokose U, Sugiura K, Ishikawa J, Akiyama M, and Kihara A (2015) Essential role of the cytochrome P450 CYP4F22 in the production of acylceramide, the key lipid for skin permeability barrier formation. Proc. Natl. Acad. Sci. USA, 112, 7707-7712.(プレスリリース原稿)
- Miyamoto M, Sassa T, Sawai M, Kihara A (2020) Lipid polarity gradient formed by omega-hydroxy lipids in tear film prevents dry eye disease. eLife, 9, e53582.(プレスリリース原稿)
- Ohno Y, Kamiyama N, Nakamichi S, Kihara A (2017) PNPLA1 is a transacylase essential for the generation of the skin barrier lipid ω-O-acylceramide. Nat Commun, 8, 14610.(プレスリリース原稿)
- Ohno Y, Nara A, Nakamichi S, Kihara A (2018) Molecular mechanism of the ichthyosis pathology of Chanarin-Dorfman syndrome: Stimulation of PNPLA1-catalyzed ω-O-acylceramide production by ABHD5. J Dermatol Sci, 92, 245-253.
- Yamamoto H, Hattori M, Chamulitrat W, Ohno Y, Kihara A (2020) Skin permeability barrier formation by the ichthyosis-causative gene FATP4 through formation of the barrier lipid ω-O-acylceramide. Proc Natl Acad Sci USA, 117, 2914-2922.(プレスリリース原稿)
- Kihara A, Igarashi Y (2002) Identification and characterization of a Saccharomyces cerevisiae gene, RSB1, involved in sphingoid long-chain base release. J Biol Chem, 277, 30048-30054.
- Kihara A, Igarashi Y (2004) Cross talk between sphingolipids and glycerophospholipids in the establishment of plasma membrane asymmetry. Mol Biol Cell, 15, 4949-4959.
- Ikeda M, Kihara A, Denpoh A, Igarashi Y (2008) The Rim101 pathway is involved in Rsb1 expression induced by altered lipid asymmetry. Mol Biol Cell, 19, 1922-1931.
- Obara K, Yamamoto H, Kihara A (2012) Membrane protein Rim21 plays a central role in sensing ambient pH in Saccharomyces cerevisiae. J Biol Chem, 287, 38473-38481.
- Ogawa C, Kihara A, Gokoh M, Igarashi Y (2003) Identification and characterization of a novel human sphingosine-1-phosphate phosphohydrolase, hSPP2. J Biol Chem, 278, 1268-1272.
- Uemura S, Kihara A, Inokuchi J, Igarashi Y (2003) Csg1p and newly identified Csh1p function in mannosylinositol phosphorylceramide synthesis by interacting with Csg2p. J Biol Chem, 278, 45049-45055.
- Mizutani Y, Kihara A, Chiba H, Tojo H, Igarashi Y (2008) 2-Hydroxy-ceramide synthesis by ceramide synthase family: enzymatic basis for the preference of FA chain length. J Lipid Res, 49, 2356-2364.
- Jojima K, Kihara A (2023) Metabolism of sphingadiene and characterization of the sphingadiene-producing enzyme FADS3. Biochim Biophys Acta Mol Cell Biol Lipids, 1868, 159335.
- Yamamoto M, Sassa T, Kyono Y, Uemura H, Kugo M, Hayashi H, Imai Y, Yamanishi K, Kihara A (2021) Comprehensive stratum corneum ceramide profiling reveals reduced acylceramides in ichthyosis patient with CERS3 mutations. J Dermatol, 48, 447-456.
- Naganuma T, Takagi S, Kanetake T, Kitamura T, Hattori S, Miyakawa T, Sassa T, Kihara A (2016) Disruption of the Sjögren-Larsson syndrome gene Aldh3a2 in mice increases keratinocyte growth and retards skin barrier recovery. J Biol Chem, 291, 11676-11688.
- Nojiri K, Fudetani S, Arai A, Kitamura T, Sassa T, Kihara A (2021) Impaired skin barrier function due to reduced ω-O-acylceramide levels in a mouse model of Sjögren-Larsson syndrome. Mol Cell Biol, 41, e0035221.
- Arai A, Takeichi T, Wakamoto H, Sassa T, Ito Y, Murase Y, Ogi T, Akiyama M, Kihara A (2022) Ceramide profiling of stratum corneum in Sjögren-Larsson syndrome. J Dermatol Sci, 107, 114-122.
